广告
英国脱欧,产品出口英国需要UKCA/英国代表/英国注册
1/3
- 面议
- 2021-09-14 09:14:30
- 有限责任公司
- 韩版
- 英国代表,UKCA 技术服务,MHRA注册
- 上海
- 上海沙格医疗科技有限公司
信息介绍
详细参数
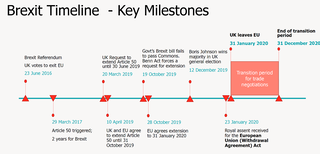
英国脱欧后,不再沿用之前欧盟框架下的市场准入的法规和制度,而建立英国自身的市场准入法规和制度 UKCA认证标志。英国脱欧的过渡期将在2020年12月31日结束。从2021年1月1日后,UKCA标志就启用了。
医疗器械的加贴UKCA标志的要求,总体上可以分为UKCA合格评定和MHRA注册申报两大模块。
1)对于目前持有公告机构签发CE证书的制造商,在 2023年6月30日之前,可以继续使用CE证书将产品出口到英国(UK)市场。在2023年6月30日之后,还可以继续出口到英国的北爱尔兰(NI)市场,而不再能出口到GB(英格兰、苏格兰和威尔士)市场。所以,从2023年7月1日开始,原来需要通过公告机构CE证书出口的医疗器械,要继续出口到GB市场,需要取得获认可的英国认证机构签发的UKCA的证书;
2)对于自我宣告类产品(依据MDD指令和IVDD指令),在2021年1月1日开始就可以按照UK MDR 2002的要求来准备技术文件和相关支持性材料,以完成自我宣告,加贴UKCA标记
更多咨询:FDA注册,FDA510K,MDR CE技术 欧代 欧盟注册,自由销售证书,英国UKCA 技术服务,MHRA注册,英国代表,ISO13485, :3咨询电话:
- 英国代表,UKCA 技术服务,MHRA注册
- 管理咨询
- 上海
- 王燕
- 有限责任公司
- 韩版
- 企业管理
上海沙格医疗科技有限公司为你提供的“英国脱欧,产品出口英国需要UKCA/英国代表/英国注册”详细介绍
英国UKCA信息
-
 矿山开采除了爆破还有什么办法¥ 7980
矿山开采除了爆破还有什么办法¥ 7980 -
 仙居光辉变压器回收-相关信息¥ 588
仙居光辉变压器回收-相关信息¥ 588 -
 内蒙古个人常年收购田黄石现金收购,当天交易—供应¥ 1000
内蒙古个人常年收购田黄石现金收购,当天交易—供应¥ 1000 -
 广西北海大运F6徐工10吨后八轮提升桥随车吊¥ 259900
广西北海大运F6徐工10吨后八轮提升桥随车吊¥ 259900 -
 海宁电缆回收(市场报价)海宁本地回收电缆¥ 68888
海宁电缆回收(市场报价)海宁本地回收电缆¥ 68888 -
 东丽燃气供暖锅炉有限公司面议
东丽燃气供暖锅炉有限公司面议